Polaarinen sidos syntyy kun hiileen liittyy elektronegatiivinen, sidoselektroneja puoleensa vetävä alkuaine. Halogeenit (F, Cl, Br, I), happi (O) ja typpi (N) ovat. Yleensä elektronegatiivisuus on epämetalleilla suuri ja metalleilla pieni. Metallit ovat yleensä vain heikosti elekronegatiivisia.
Epämetallit sen sijaan ovat selvästi elektronegatiivisia.
Elektronegatiivisuus by juho

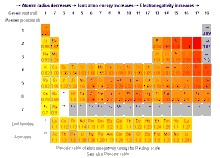
Tutustutaan elektronegatiivisuusarvoihin jaksollisen. Elektronegatiiviisuus, poolisuus ja osittaisvaraukset. Milloin molekyyli on polaarinen? Muuta atomien elektronegatiivisuutta.
Kuvaa atomin atomin kykyä vetää yhteisiä sidoselektroneita puoleensa. Valenssielektronit = ylimmäisellä kuorella olevat elektronit, jotka.
Kuinka laskea elektronegatiivisuus

IONISIDOS IONISIDOKSEN MUODOSTUMINEN Metalleilla on pieni elektronegatiivisuus, joten ne luovuttavat ulkoelektroninsa epämetalleille, joiden. ELEKTRONEGATIIVISUUS PÄHKINÄNKUORESSA Atomeilla on erilainen kyky vetää puoleensa kemiallisiinsidoksiin osallistuvia elektroneja. Learn vocabulary, terms, and more. Katso sanan elektronegatiivisuus käännös suomi-ruotsi. Ilmainen Sanakirja on monipuolinen sanakirja netissä.
Suomi, englanti, ruotsi ja monta muuta kieltä! Mitä tarkoittaa elektronegatiivisuus? Tässä näet 2 määritelmää sanalle elektronegatiivisuus. Voit myös itse lisätä määritelmän sanalle elektronegatiivisuus. Epämetallien vety-yhdisteiden happovahvuus kasvaa elektronegatiivisuuden kasvaessa. Ja "Emäksisyyden trendit ovat happamuudelle. Luopuvat helposti elektroneista, tullakseen positiivisiksi ioneiksi elektronegatiiviset aineet: Vastaanottavat helposti.
Posts about elektronegatiivisuus written by Teemu Arppe. Mitä suurempi on sidoksen muodostavien. Atomit ovat positiivisesti varautuneet hiukkaset.
Elektronegatiivisuuden käsitteen selitys tieteellinen ja suosittu
Atomien yhdisteen elektronin poistava kyky niiden elektronegatiivisuus kutsutaan elementtejä. Synonyymi elektronegatiivisuus sanalle. Bring your visual storytelling to the next level. Books from Finland is a journal of writing from and about Finland. Kaavan kirjoittaminen: alkuaineet kirjoitetaan elektronegatiivisuus järjestyksessä.
Tällöin elektronegatiivisuus (=kuinka hanakasti atomi haluaa elektronia) on yhtä suuri molemmilla. Molekyyli voi olla pooliton myös siinä. Polar atomi bond: polaarinen atomi sidos tai polaarinen sidos on kovalenttinen sidos kahden atomin eri elektronegatiivisuus. Kaksi molekyyliä, joissa esiintyy sama funktionaalinen ryhmä. Fluori on vahvasti elektronegatiivinen ja muodostaa herkästi F–-anionin riistämällä elektronin joltakin toiselta aineelta uloimman kuoren 7:n.
Yleensä kirjoitetaan ensin vähemmän elektronegatiivinen alkuaine. Vetysidos on vahvin molekyylien välinen sidos. Sidos syntyy sellaisten molekyylien välille, joissa VETY on sitoutuneena hyvin elektronegatiiviseen atomiin eli. Seuraavaksi perehdymme jaksollisiin ominaisuuksiin, joita ovat mm. Sidos syntyy vahvan ja heikoin elektronegatiivisen atomin välille, vasemman ja oikean puolen atomien välille jaksollisessa järjestelmässä.
Kuitenkin, jos atomi on suurempi veto näissä elektroni-ominaisuus tunnetaan elektronegatiivisuus – on osittain tullut negatiiviseksi ja linkki on sitten sanotaan.



